Hoá học 9 Bài 44: Rượu etylic
Rượu Etylic:
- Công thức phân tử: C2H5OH
- Nguyên tử khối: 46
a) Khái niệm
- Rượu Etylic là chất lỏng không màu, nhẹ hơn nước.
- Sôi ở 78,3oC.
- Nhẹ hơn nước và tan vô hạn trong nước. Rượu Etylic hòa tan được nhiều chất như iot, benzen…
b) Độ rượu là gì? Cách tính độ rượu.
- Độ rượu là số ml rượu Etylic nguyên chất có trong 100ml hỗn hợp rượu Etylic với nước.
Hình 1: Cách pha chế rượu 450
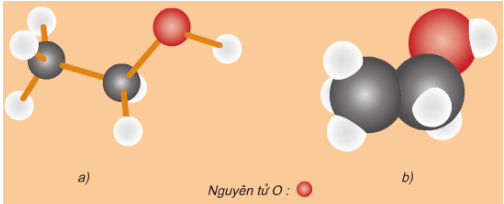
Hình 2: Mô hình phân tử rượu etylic
a)Dạng rỗng; b)Dạng đặc
- Rượu Etylic có công thức cấu tạo thu gọn là CH3 - CH2 - OH
- Trong phân tử rượu Etylic có một nguyên tử Hidro không liên kết với nguyên tử Cacbon mà liên kết với nguyên tử Oxi tạo ra nhóm - OH. Chính nhóm - OH này làm cho rượu có tính chất hóa học đặc trưng.
a) Rượu etylic có cháy không?
- Cách tiến hành: Các em chú ý quan sát thí nghiệm sau đây
Video 1: Rượu etylic cháy với Oxi
- Hiện tượng: Rượu etylic cháy với ngọn lửa màu xanh, tỏa nhiều nhiệt.
- Giải thích: Rượu etylic tác dụng với oxi khi đun nóng theo phương trình C2H6O(l) + 3O2(k) → 2CO2(k) + 3H2O(h)
b) Rượu etylic có tác dụng với Natri không?
- Cách tiến hành: Các em chú ý quan sát thí nghiệm sau
Video 2: Rượu etylic tác dụng với Natri
- Hiện tượng: Mẩu natri tan dần và có bọt khí thoát ra
- Giải thích: Natri phản ứng với rượu etylic giải phóng khí H2 theo phương trình 2CH3-CH2-OH + 2Na → 2CH3-CH2-ONa + H2
- Cách tiến hành: Các em chú ý quan sát thí nghiệm sau
Video 3: Rượu etylic tác dụng với Axit axetic
- Hiện tượng: Trong ống nghiệm có chất lỏng không màu, mùi thơm, không tan trong nước, nổi trên mặt nước.
- Giải thích: Rượu etylic tác dụng với axit axetic tạo etyl axetat theo phản ứng
C2H5OH + CH3COOH CH3COOC2H5 + H2O
Hình 3: Ứng dụng của Rượu etylic
- Phương pháp 1: Tinh bột hoặc đường (overset{len men}{rightarrow}) rượu Etylic
Hình 4: Quy trình chế rượu etylic bằng phương pháp lên men rượu
- Phương pháp 2: C2H4(k) + H2O(l) (overset{Axit}{rightarrow}) C2H5OH
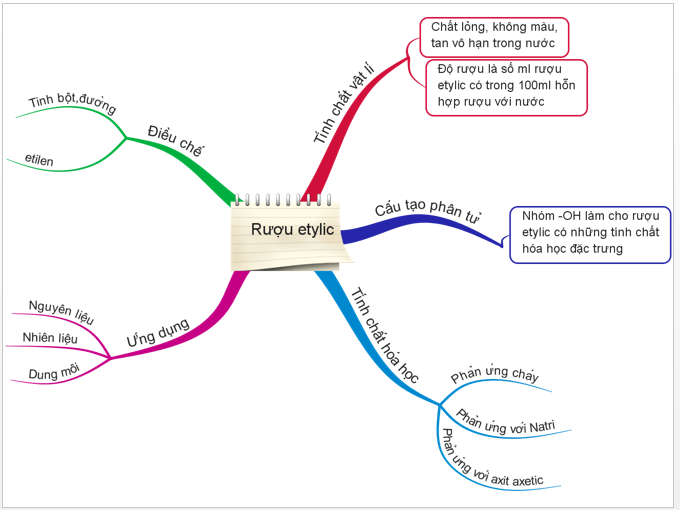
Hình 5: Sơ đồ tư duy bài Rượu Etylic
Link nội dung: https://cdsphagiang.edu.vn/index.php/ruou-etylic-hoa-9-a91913.html